Урок химии в 8 классе
Выполнила: учитель химии высшей категории Кобытева Е.И.
Цели. Сформировать представление о классификации неорганических веществ; проследить зависимость состава соединений и их химического характера; продолжить формирование умений составлять формулы оксидов по степени окисления, давать названия оксидам; познакомить учащихся с применением оксидов в быту и промышленности; формировать бережное отношение к природным богатствам; развивать навыки работы с веществами; развивать логическое мышление учащихся.
Оборудование и реактивы. Мультимедийный проектор; видеомагнитофон;
на столах учащихся: CuO, SiO2,Cr2O3, пробирка с СО2, стаканчики с водой, стеклянные палочки.
ХОД УРОКА
1этап. Целеполагание
Что мы узнаем? Чему мы научимся?
(план урока)
- Как классифицируют вещества? Составлять формулы оксидов.
- Как отличить оксиды от других веществ? Определять характер оксидов
- Какие бывают оксиды? по формуле.
- Где применяются оксиды?
2 этап. Классификация неорганических веществ
 Беседа с учащимися с составлением схемы (слайд 1).
Беседа с учащимися с составлением схемы (слайд 1).
Оксиды – бинарные соединения элементов с кислородом в степени окисления -2.
Проверь себя: Na2O; P2O5; CaO; SO3.
3 этап. Классификация оксидов
Вопрос: Подумайте, по какому признаку можно классифицировать оксиды? (Посмотрите на классификацию простых веществ).
Основные оксиды – оксиды металлов, которым соответствуют основания.
Кислотные оксиды – оксиды неметаллов, которым соответствуют кислоты.
5 этап. Физические свойства оксидов
Практическая работа. Рассмотрите образцы оксидов. Результаты наблюдений занесите в таблицу.
| Название оксида | Химическая формула | Цвет | Агрегатное состояние | t°плавления, °C | Строение(молекулярное или немолекулярное) |
| Оксид меди (II)Оксид магнияОксид хрома (III)Оксид кремнияОксид водородаОксид углерода (IV) | CuOMgOCr2O3SiO2H2OCO2 | > 1000 разлагается2800156517130-56,6 |
Вывод: оксиды металлов — твердые вещества немолекулярного строения, оксиды неметаллов могут быть как молекулярного строения, так и немолекулярного. Свойства веществ зависят от строения.
6 этап. Применение оксидов
1.Оксид водорода – вода (Н2О)
О воде пишут песни, слагают стихи. Вот, например, стихотворение Л.Мартынова, которое так и называется: «Просто вода». (Фрагмент видеофильма о воде, чтение стихов).
Л. Мартынов
Вода – самое распространенное вещество на планете.
Запасы воды на Земле 1млн 454тыс м3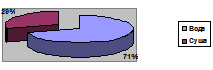
из них менее 2% относится к пресным водам, доступны для использования 0,3%.
Расход воды в мире
(в м3 на человека в сутки)
Анализ диаграммы.
Обсуждение, для каких целей используется вода в быту.
В промышленности:
1т синтетического волокна- 2000м3 воды;
1т газетной бумаги – 900м3 воды.
Вывод: необходимо очень экономно и рационально расходовать природные ресурсы.
2.Оксид кремния(IV)- SiO2
Перед вами хорошо известный речной песок. Это и есть SiO2.
Опишите физические свойства оксида кремния (IV).
(ответы учащихся).
УЧИТЕЛЬ: Но оксид кремния — это не только речной песок. 
- Кварц, кремень, горный хрусталь, аметист, яшма, опал — все это оксид кремния (IV). (иллюстрации).
Это были оксиды неметаллов. Теперь рассмотрим Один из оксидов металлов.
3.Оксид хрома (III)
УЧИТЕЛЬ: Этот оксид можно получить в лаборатории с помощью очень интересного опыта. Он называется «Извержение вулкана».
Просмотр видеофильма. Обсуждение.
Опишите физические свойства оксида хрома (III).
Применение оксида хрома(Ш):
- Используют как пигмент при изготовлении декоративного зеленого стекла, керамики, зеленой краски (хромпик).
- Паста ГОИ (“Государственный оптический институт”) на основе Cr2O3 применяется для шлифовки и полировки оптических изделий, в ювелирном деле.
Демонстрация: ваза из зеленого стекла (Дятьковский хрустальный завод); паста ГОИ.
УЧИТЕЛЬ: О применении оксидов можно говорить еще очень много, но время урока ограничено. Вы можете найти материал о применении других оксидов и подготовить сообщение к следующему уроку.
7 этап. Обобщение изученного на уроке
УЧИТЕЛЬ: Наш урок подходит к концу. Давайте посмотрим, все ли удалось, что мы планировали.
(Возврат к плану урока, анализ – все ли цели достигнуты).
8 этап. Закрепление на более высоком уровне
ПРОВЕРЬ СЕБЯ.
Задание. Исключи лишнее вещество:
CO2, NaOH, CaO, SiO2. (учащиеся исключают NaOH, аргументируют ответ).
УЧИТЕЛЬ: Что общего у оставшихся веществ? (оксиды).
Давайте заменим NaOH на Р2О5. Теперь все вещества – оксиды.
Что теперь лишнее? Почему? (СаО – основный, остальные – кислотные).
9 этап. Домашнее задание.
Вам пригодилась эта разработка? Напишите «Спасибо» учителю: